LAL-Test
Um Endotoxine quantitativ ermitteln zu können wurde der Limulus-Amöbocyten-Lysat-Test, kurz LAL-Test entwickelt. Das Ergebnis wird in Endotoxin Units pro ml (EU/ml) angegeben. Ein 1 EU/ml entsprechen 0,1 ng Endotoxine pro ml getestete Lösung.
Der LAL-Test beruht auf der Beobachtung, dass eine Infektion des Pfeilschwanzkrebses (Limulus polyphemus) mit gramnegativen Bakterien zur Blutgerinnung führt. Diese Koagulation wird durch eine Reaktion des bakteriellen Endotoxins mit einem Gel-bildenden Protein in den Blutzellen (Amoebozyten) des Tieres hervorgerufen. Für den LAL-Test wird aus dem Blut der Pfeilschwanzkrebse ein Lysat gewonnen, in dem dieses gerrinungsfördernde Protein als inaktive Vorstufe vorliegt. Kommt diese inaktive Vorstufe mit Endotoxinen gramnegativer Bakterien in Berührung, wandelt es sich in aktives Enzym um (siehe Abbildung). Die Aktivierung des Enzyms setzt im LAL-Test durch eine Reaktion mit einem chromogenen Substrat, an das ein gelber Farbstoff (p-Nitroanilin) gekoppelt ist, diesen frei. Die Freisetzung von Farbstoff steht in direktem Zusammenhang mit der Menge an Endotoxin in der Testlösung. Somit wird eine indirekte photometrische Bestimmung der Enzymaktivität ermöglicht.
Die Aktivität wird mithilfe der optischen Dichte (OD) gemessen. Der Endotoxin-Wert in EU/ml berechnet sich aus der OD405 mit Hilfe einer Standardgerade.
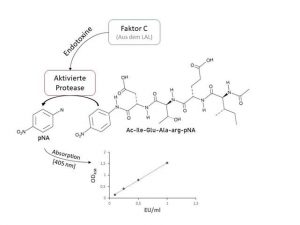
Abbildung : Ein kleines Volumen der Probe (10μL) wird mit dem Limulus-Amöbozyten-Lysat kombiniert. In der Probe vorhandene Endotoxine aktivieren die proteolytische Aktivität von Faktor C im LAL. Die Aktivität von Faktor C wird durch Zugabe von chromogenem Substrat gemessen. Der abgespaltene p-Nitroalinin (pNA)Rest kann durch Messung der Absorption bei 405nm gemessen werden. Extrapolation gegen eine Standardkurve erlaubt die Quantifizierung von EU/ml.
